新闻网讯 中央民族大学程勇教授团队近日在《Research》期刊上发表了题为“Targeted Delivery of Engineered RVG-BDNF-Exosomes: A Novel Neurobiological Approach for Ameliorating Depression and Regulating Neurogenesis”的研究论文,介绍了一种新型靶向神经元的工程化外泌体及其结合基因治疗的技术。工程化外泌体能穿越血脑屏障,将脑源性神经营养因子(BDNF)靶向传递至大脑神经元,不仅促进了突触的可塑性,还减轻了脑部炎症,显著改善了小鼠的抑郁症状。这一研究为抑郁症的治疗提供了新的策略和方向。(Research,2024,Doi:10.34133/research.0402)。
Citation: Liu S, Chen L, Guo M, Li Y,Liu Q, Cheng Y. Targeted Delivery of Engineered RVG-BDNF-Exosomes: A Novel Neurobiological Approach for Ameliorating Depression and Regulating Neurogenesis. Research 2024. https://doi.org/10.34133/research.0402
研究背景
抑郁症是一种常见且严重的精神疾病,表现为持续的情绪低落、兴趣丧失和认知功能障碍。根据神经营养因子假说,抑郁症的发生与BDNF的水平密切相关。BDNF在神经元的发育、分化和存活中起着至关重要的作用,并在神经可塑性和抑郁症的发病机制中扮演重要角色。研究表明,抑郁症患者大脑中BDNF的表达水平显著降低,特别是在前额叶皮层和海马区域,这与抑郁症的发生密切相关。此外,大量临床前研究表明,BDNF可能是治疗抑郁症的重要靶点。
尽管BDNF被认为是治疗抑郁症的重要靶点,但其应用受到血脑屏障(BBB)的限制。BBB是一种选择性渗透屏障,能够保护大脑免受有害物质的侵害,但同时也限制了治疗药物,特别是大分子药物如BDNF,进入大脑。此外,如何将BDNF精确地靶向到特定的神经元也是一大难题。这些因素都限制了BDNF在临床治疗中的广泛应用。
近年来,外泌体作为一种新型纳米载体在生物医学领域得到了广泛关注。外泌体是由细胞分泌的,直径在30至150纳米之间,能够封装多种生物活性成分,并在细胞间传递物质和信息。研究发现,外泌体在抑郁症的病理过程中发挥了重要作用,能够调节神经炎症和神经可塑性。更为重要的是,外泌体较易通过血脑屏障从外周进入大脑,尤其是改装后的外泌体具备很强的靶向性,能够将药物或基因物质递送到大脑特定部位或特定细胞。
研究进展
程勇教授课题组通过基因工程技术开发出一种能够高效递送BDNF基因的靶向外泌体。具体来说,他们将神经元特异性的狂犬病毒糖蛋白(RVG)和BDNF基因结合,并导入到293T细胞中。这些细胞随后生产出含有BDNF基因的工程化外泌体(RVG-BDNF-Exos),能够特异性地靶向神经元。
为了验证这些工程化外泌体的特性,研究人员使用了纳米粒子追踪分析、电镜、qRT-PCR和Western blot等技术,结果显示外泌体的直径大约为131纳米,并且成功整合了目标蛋白质。此外,研究团队通过尾静脉注射将标记后的外泌体注入小鼠体内,发现这些外泌体能够有效地靶向小鼠大脑中的神经元,证明了它们在体内的靶向效果(图1)。
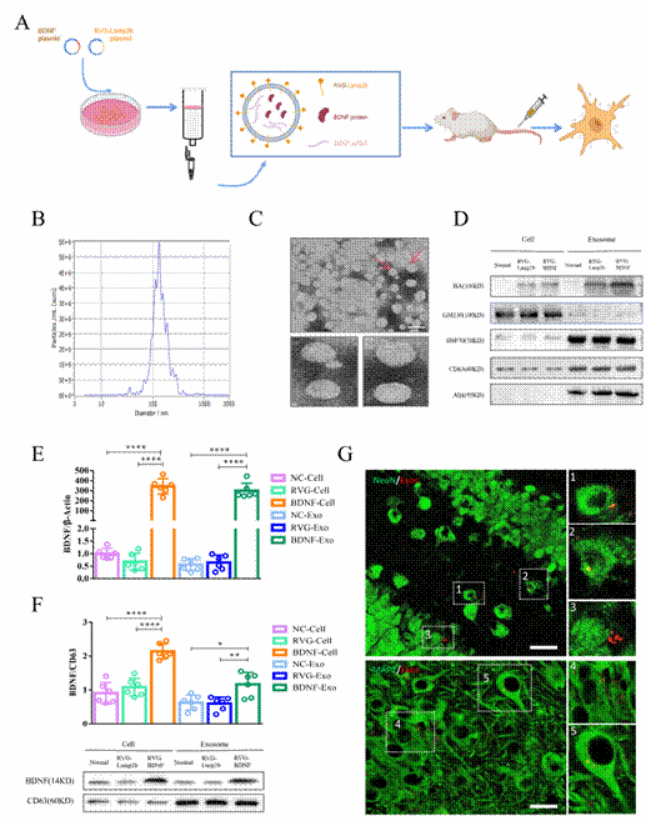
图 1. 工程化外泌体的特性表征
为了评估RVG-BDNF-Exos在大脑中递送BDNF的效果,研究人员使用抑郁样行为小鼠进行了实验。结果显示,接受RVG-BDNF-Exos治疗的小鼠在海马和前额叶皮层区域的BDNF蛋白水平显著提高,并激活了下游信号通路,减少了炎症反应,证明了工程化外泌体在体内激活了BDNF信号通路(图2)。
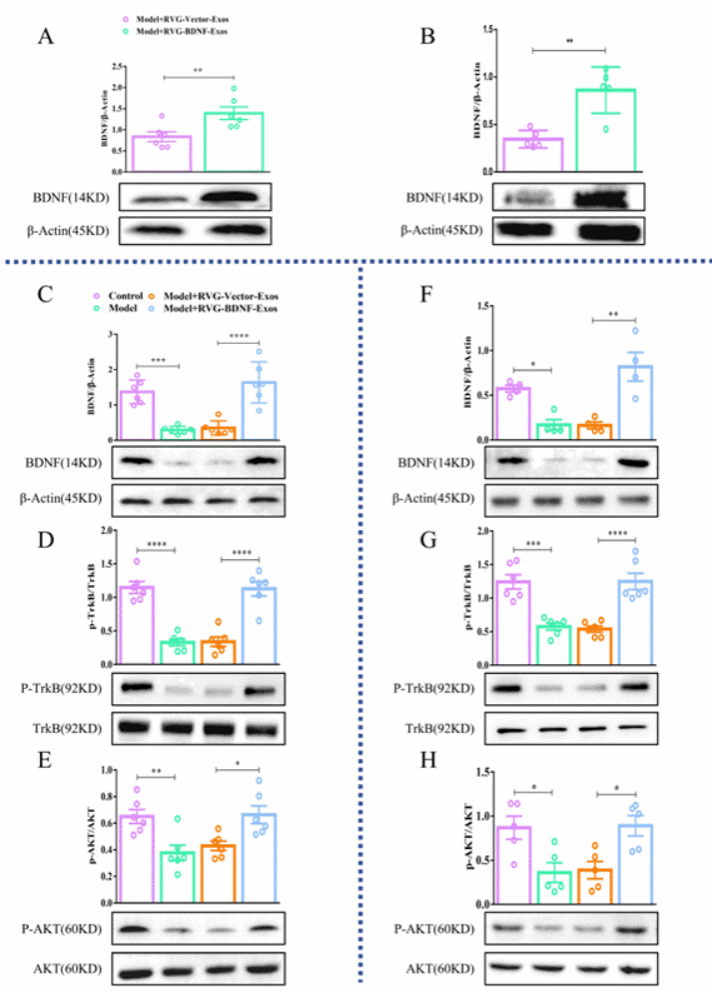
图2. RVG-BDNF-Exos促进海马和前额叶皮层中的 BDNF/TrkB 信号转导
在一系列行为学测试中,接受RVG-BDNF-Exos治疗的小鼠表现出显著的抑郁症状改善。例如,在旷场测试中,小鼠的静止时间显著减少;在强迫游泳测试和尾悬测试中,小鼠的静止时间也显著缩短;在新奇食物抑制测试中,小鼠在新环境中的进食潜伏期明显缩短。这些结果表明RVG-BDNF-Exos能够显著改善抑郁样行为(图3)。
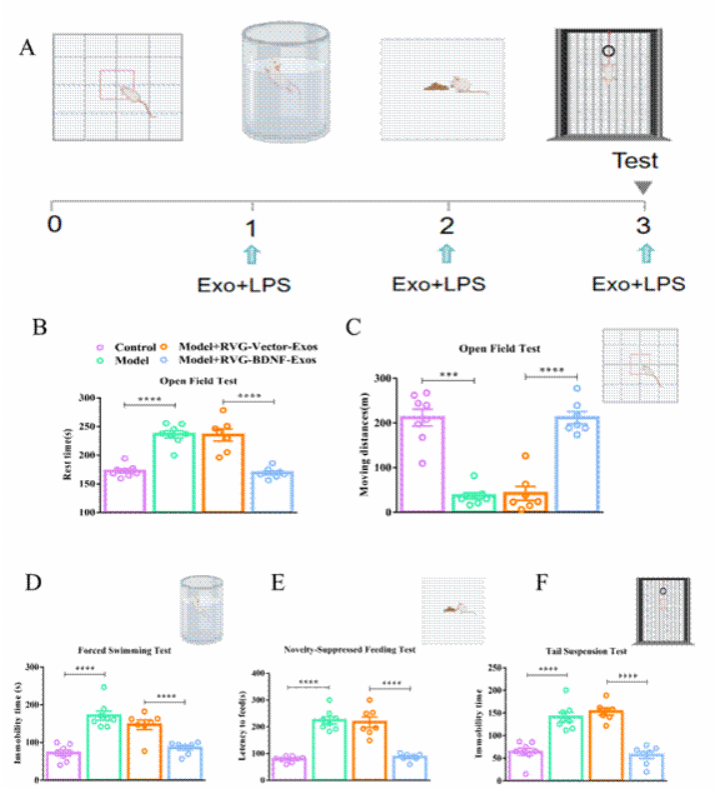
图 3. 工程化外泌体可显著改善小鼠抑郁样行为
进一步的研究发现,RVG-BDNF-Exos不仅能够减少抑郁样行为小鼠脑部的小胶质细胞数量,缓解神经炎症,还显著降低了星形胶质细胞的数量,这些结果进一步表明其对抑郁症有显著的治疗潜力(图4、图5)。
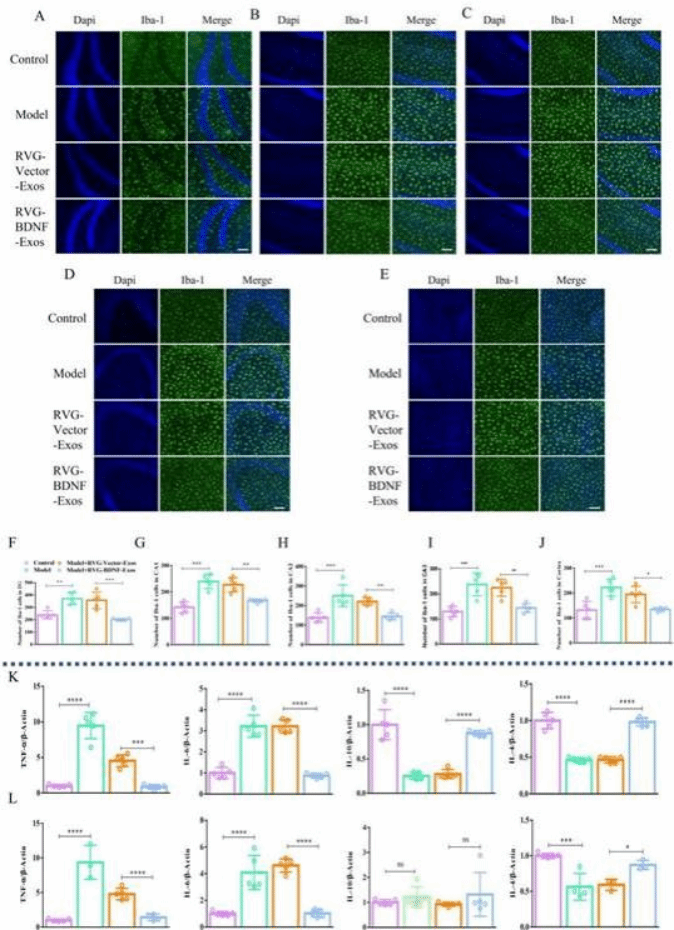
图4. RVG-BDNF-Exos 可减轻抑郁样行为小鼠的小胶质细胞数量和神经炎症
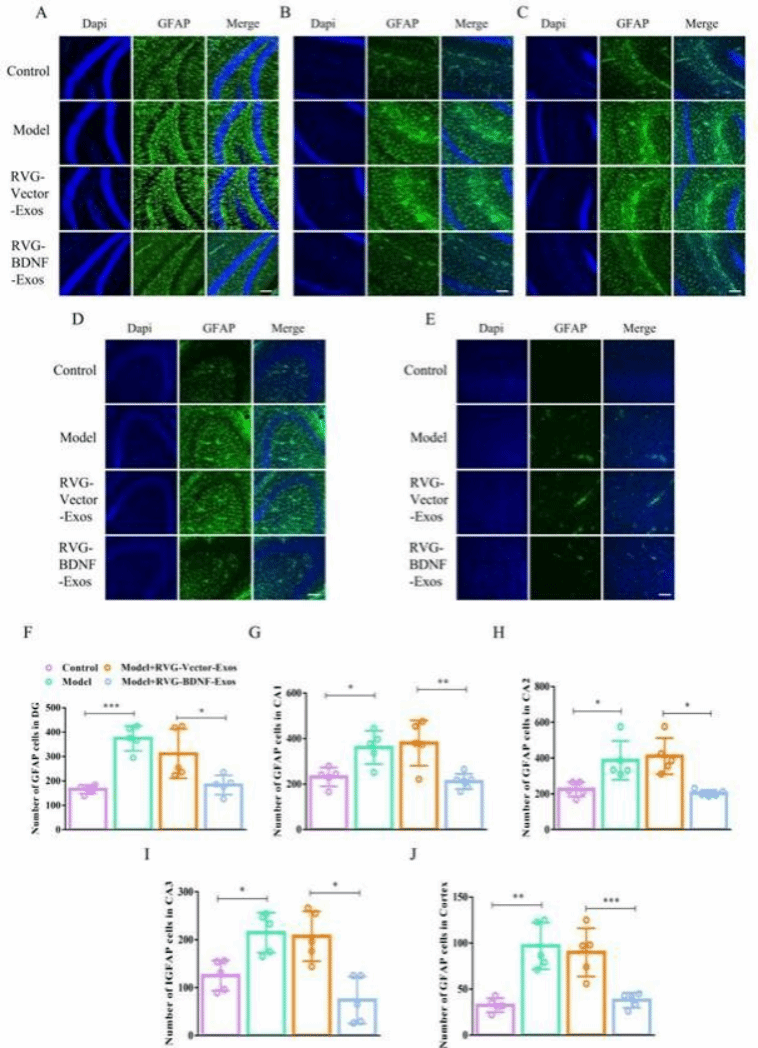
图5. RVG-BDNF-Exos可减少抑郁样行为小鼠的星形胶质细胞数量
此外,RVG-BDNF-Exos治疗显著增加了小鼠海马和前额叶皮层区域的成熟神经元数量,并提高了神经发生的标志物DCX的表达。在突触可塑性方面,研究发现RVG-BDNF-Exos能够显著提高海马和前额叶皮层区域的突触相关蛋白PSD95和Syn-1的表达水平。这些结果表明RVG-BDNF-Exos可能通过促进神经发生和调节突触可塑性来增强抑郁症的治疗效果(图6)。
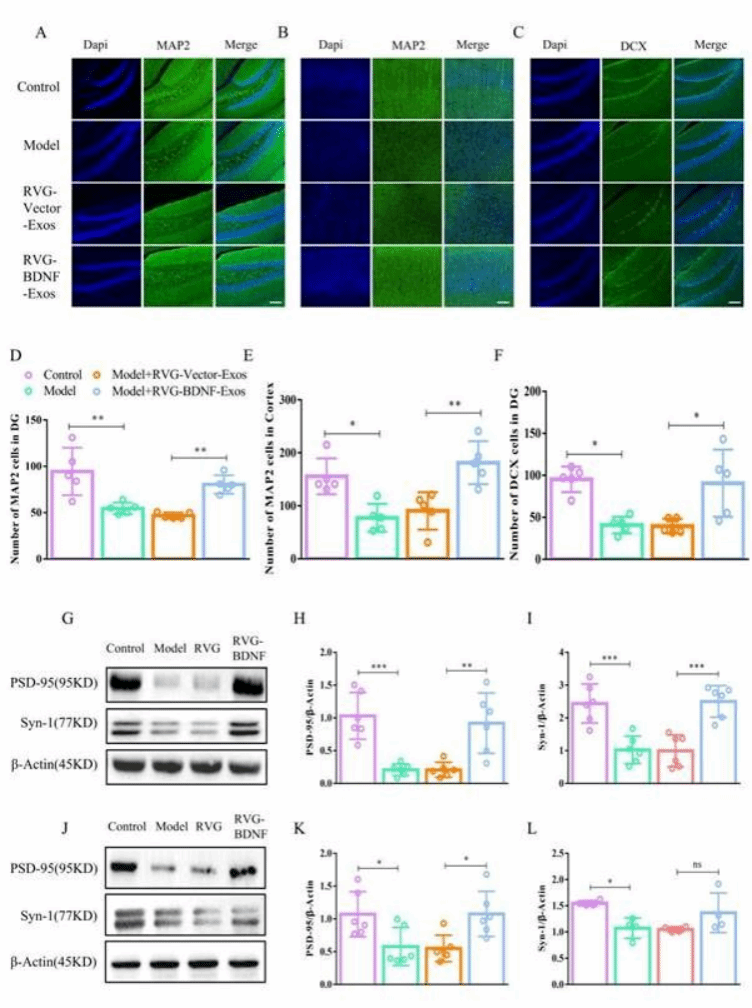
图6. RVG-BDNF-Exos能增强神经发生和调节突触可塑性
未来展望
程勇教授团队的这一研究不仅为抑郁症的治疗提供了新的策略,也为神经系统疾病的基因治疗开辟了新的路径,具有广阔的应用前景和巨大的研究价值。未来,团队将继续深入探索这一技术在生物医学研究中的潜力,并努力将其转化为临床应用,为更多患者带来希望。
